Tu es tous les jours au contact de l’eau, que ce soit sous la douche, sous la pluie ou pour la boire, mais as-tu déjà remarqué les différentes formes qu’elle pouvait prendre dans l’environnement ?
Nous allons parler des trois formes (états) que peut prendre l’eau et comment cela est possible.
A la fin de cet article, je te propose de réaliser un petit test pour répondre à une question que je vais te poser.
Les trois états de l’eau
Quelques cas particuliers
Passage d’un état à l’autre
Variation de volume en fonction des états
Petite expérience
Zoom sur l’eau
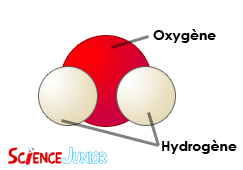
Commençons par faire un énorme zoom sur l’eau, a un tel point que l’on peut voir ses molécules. Les molécules d’eau sont des sortes de briques qui, lorsqu’elles seront ensemble, vont former de l’eau. Une molécule d’eau est toujours constituée d’un atome d’Oxygène (O) et de deux atomes d’hydrogène (H). Ils sont toujours assemblés de la même façon.
Les trois états de l’eau
L’eau peut exister à l’état :
solide : c’est la glace, le verglas… Les molécules d’eau sont parfaitement organisées de façon à former quelque chose de dure et solide.
liquide : c’est l’eau des rivières, de l’océan, du robinet, même des nuage ! Les molécules d’eau sont un peu dans tous les sens, mais assez proches les unes des autres.
gazeux : c’est de l’eau qui n’est pas visible à l’œil nu. Il y en a partout dans l’air que l’on respire. Les molécules d’eau sont désordonnées et très espacées les unes des autres.
- Zoom sur de l’eau à l’état gazeux
- Zoom sur de l’eau à l’état liquide
- Zoom sur de l’eau à l’état solide
Quelques cas particuliers
La vapeur d’eau : la « vraie » vapeur d’eau est totalement invisible à l’œil nu. C’est donc de l’eau à l’état gazeux. On la retrouve partout (sans la voir) dans l’air que nous respirons. Elle se forme par exemple par l’évaporation des océans, des lacs, etc…
Les nuages : il s’agit d’eau à l’état liquide. C’est en fait de l’eau en très petites particules, tellement petites qu’elles arrivent à flotter dans l’air pour former des nuages. Ces particules qui forment les nuages ce sont formées à partir de la vapeur d’eau contenue dans l’air.
La « vapeur » d’eau de la cocotte-minute : La fumée que l’on voit s’échapper de la cocotte-minute ou de la bouilloire n’est en réalité pas de la vapeur d’eau. C’est un abus de langage. Cette fumée est, tout comme les nuages, constituée de fines particules d’eau qui flottent dans l’air. C’est donc de l’eau liquide. En fait, l’eau de la bouilloire est tellement chauffée qu’elle s’évapore (elle devient de la vapeur), et presque immédiatement, au contact de l’air plus froid, se condense pour former cette sorte de fumée.
Passage d’un état à l’autre
L’eau peut changer d’état à tout moment, il faut juste que certaines conditions soient présentes. En fonction de la température, l’eau peut prendre différente forme.
Par exemple, pour que l’eau passe de l’état liquide à solide, la température doit passer en dessous de 0°C (zéro degré Celsius). Ce phénomène est réversible, c’est à dire que si la température redevient supérieure à 0°C, l’eau redevient liquide.
Mais le passage d’un état à l’autre n’est pas immédiat : à 0°C, il y aura un peu d’eau liquide et un peu d’eau solide, le temps que toute l’eau liquide devienne solide.
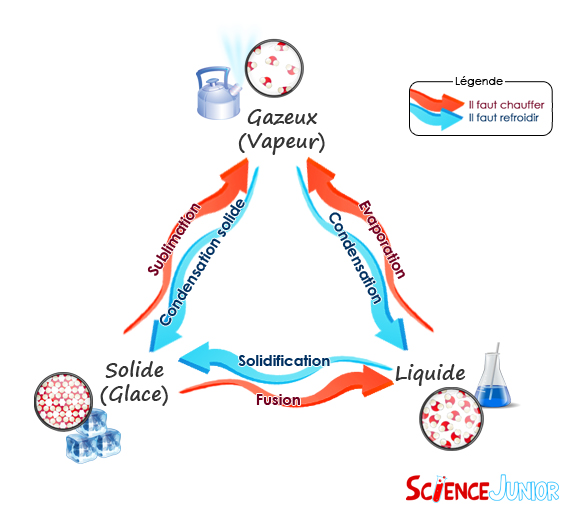
Les passages d’un état à l’autre portent des noms :
La condensation : c’est le passage de l’état gazeux à liquide. Il existe également la condensation solide, qui est le passage de l’état de gaz à solide, sans passer par la phase liquide.
L’évaporation : c’est le passage de l’état liquide à l’état gazeux.
La fusion : c’est le passage de l’état solide à liquide.
La sublimation : c’est le passage directement de l’état solide à l’état gazeux. Cela se produit dans certaines conditions de pression.
La solidification : c’est le passage de l’état liquide à solide.
Les voici sous forme d’un schéma :
Variation de volume en fonction des états
L’eau liquide occupe un certain volume. En changeant d’état, l’eau sous forme solide (la glace) ou sous forme de gaz (la vapeur) va occuper un volume différent.
Le volume occupé par l’eau à l’état gazeux est plus grand que celui de l’eau à l’état liquide. En effet, ses molécules vont se disperser sans s’arrêter pour essayer d’occuper le plus grand espace possible.
L’eau à l’état solide va également occuper un volume plus grand que l’eau à l’état liquide mais contrairement au volume de la vapeur, celui de l’eau solide va s’arrêter de grandir lorsque toute l’eau est devenue solide.
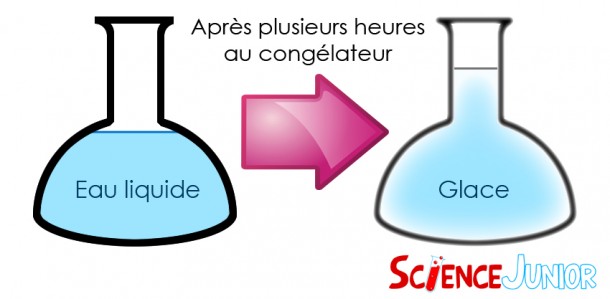
Tu peux d’ailleurs faire le test toi-même.
Mets de l’eau à la moitié d’un verre et fais un repère pour savoir quel volume d’eau tu as mis. Place le verre au congélateur plusieurs heures. Tu verras que la glace a monté !
Petite expérience
Sais-tu si l’eau change de poids lorsqu’elle passe de l’état liquide à solide ?
Pour répondre à cette question, tu peux faire une petite expérience :
Mets 100 grammes d’eau dans un verre en plastique et place-le au congélateur. Quelle est la masse du glaçon obtenu ?
Voici la réponse :
Le glaçon pèse aussi 100 grammes, autant que la masse d’eau mise au départ dans le verre ! Les molécules d’eau se sont « rangées » de façon à former de la glace, mais elles sont toutes là, aucune n’a été perdue, et aucune n’est apparue. Par conséquent, la masse totale de toutes les molécules reste la même. Et c’est la même chose dans l’autre sens ; si tu fais fondre le glaçon obtenu et que tu pèses la masse d’eau, tu auras toujours 100 grammes d’eau : les molécules se sont désorganisées donc le volume est plus petit, mais aucune n’a été perdue.